人類吸大麻后,大腦里發生了什么?關于這一問題,上海科學家有了最新研究成果,并且這一研究成果對疼痛炎癥和尼古丁成癮等疾病的藥物開發很有幫助。7月6日凌晨,這項成果在國際頂尖學術期刊《自然》(《Natur
人類吸大麻后,大腦里發生了什么?
關于這一問題,上海科學家有了最新研究成果,并且這一研究成果對疼痛炎癥和尼古丁成癮等疾病的藥物開發很有幫助。
7月6日凌晨,這項成果在國際頂尖學術期刊《自然》(《Nature》)上發表,并作為重點文章推介。該研究是上海科技大學iHuman研究所繼2016年10月首次發表大麻素受體CB1與拮抗劑復合物的高分辨率三維結構之后的又一重大突破。
澎湃新聞(www.thepaper.cn)記者從上海科技大學獲悉,這次的研究成果呈現了人類吸大麻后,大腦內大麻素受體與大麻的成癮性物質四氫大麻酚(THC)是如何相互作用的,簡單說,搞清楚了四氫大麻酚類激動劑小分子對大腦內中樞神經系統里的大麻素受體是如何調控的。
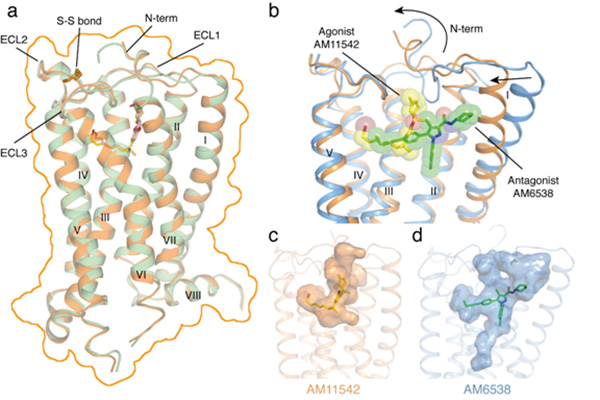
CB1與激動劑復合物的三維結構(a);激動劑與拮抗劑小分子結合方式及結合口袋比較(b-d, 藍色: 與拮抗劑AM6538結合的受體;橙色: 與激動劑AM11542結合的受體)。 本文圖均為上科大供圖
搞清了人體內大麻素受體的“陰陽兩面”
大麻素受體CB1是人體中樞神經系統表達量最高的GPCR之一,它對人的精神和情緒調節至關重要。
2016年10月,iHuman研究所團隊率先在國際學術期刊《細胞》(《Cell》)上發表了人源大麻素受體CB1與拮抗劑小分子AM6538復合物的高分辨率三維結構,該結構揭示了CB1在非活化狀態下的構象以及拮抗劑小分子與受體之間的作用模式,對設計更加特異、副作用更小的拮抗劑類藥物,比如肥胖、及肥胖引起的代謝類疾病,肝纖維化及尼古丁成癮等疾病,具有極大的促進作用。
大麻素受體CB1的激動劑在疼痛、炎癥、多發性硬化癥及神經退行性疾病等的治療中有非常大的潛力,但激動劑小分子,例如大麻里的主要精神類成分THC,是如何與CB1相互作用以及受體的活化機制等尚不清楚。
目前已解析的GPCR三維結構中大部分是與拮抗劑配體的復合物,與激動劑結合的活化狀態的GPCR構象非常活躍且不穩定,解析其復合物結構的難度相對較大。
為獲得大麻素受體CB1與激動劑復合物的三維結構,iHuman研究團隊與美國東北大學的Makriyannis實驗室合作,成功解析了大麻素受體CB1與兩種新型激動劑小分子AM11542和AM841復合物的三維精細結構。
該結構不僅揭示了激動劑小分子與CB1的相互作用模式,更重要的是,研究者發現,這與之前解析的CB1-拮抗劑小分子復合物結構相比,發生了很大的構象變化。這些結構特征也從分子水平解釋了,為何大麻素受體CB1可與多種不同類型的配體相互作用,參與和調控人體中多種非常重要的生理活動,也為今后針對GPCR的藥物設計提供了新的思路。
該研究的另一重要發現是,首次從三維結構上觀測到兩個氨基酸在受體激活過程中的協同構象變化,這一變化可能與CB1的活化機制密切相關。
“掌握了CB1與激動劑和拮抗劑復合物的三維結構信息,或者說看清了這個受體的‘陰陽雙面’,不僅對于內源性大麻素系統的功能機制研究極其重要,對一系列疾病,如炎癥、疼痛和多發性硬化癥等的藥物研發有重要的指導意義。” iHuman研究所副所長劉志杰教授表示,由于大麻濫用及合法化等問題,該研究也有非常重要的社會價值,“我們很高興能取得了這個歷史性突破。”

iHuman研究團隊部分成員合影。從左至右:濮夢辰,吳屹然,劉志杰,華甜,Raymond Stevens,曲露,丁康。
第一作者華甜:為這項研究主動推遲博士畢業
該項研究由iHuman研究所副所長、教授劉志杰課題組,創始所長、特聘教授Raymond Stevens課題組,iHuman研究所研究副教授、生命學院助理教授趙素文課題組及其它合作單位共同完成。劉志杰、趙素文是論文的共同通訊作者,劉志杰課題組博士研究生華甜(與中科院生物物理研究所聯合培養)是論文第一作者,上科大是第一完成單位。
值得一提的是,這也是博士研究生華甜繼2016年10月發表在《Cell》后,作為第一作者取得的第二項重大科研成果,“其實這項研究在去年向《Cell》投稿前后就開始了,是同步進行的,為了及時攻克CB1與激動劑復合物的晶體結構,我主動把博士畢業的時間延后了一年。”華甜說。
華甜的導師劉志杰表示,華甜的成功并不意外,她十分刻苦,幾乎每天在實驗室工作17個小時,春節只回家幾天就匆匆趕回上海的實驗室。




